



Reportagem: Aline Tavares
Fotos: André Ricoy e José Felipe Batista/Comunicação Butantan
Em 2006, o cientista Isaías Raw (1927-2022), ex-diretor do Instituto Butantan e da Fundação Butantan, convidou para uma reunião pesquisadores do Instituto Nacional de Alergia e Doenças Infecciosas (NIAID), parte dos Institutos Nacionais de Saúde (NIH) dos Estados Unidos. O motivo: entender a tecnologia que a organização norte-americana vinha desenvolvendo com vistas a obter uma candidata vacinal contra a dengue. Naquele ano, a doença atingia níveis históricos na região das Américas, com 260 mil casos prováveis só no Brasil, e Isaías enxergava a necessidade de se ter um imunizante nacional para proteger a população da dengue. Vinte anos e muito trabalho depois, a Butantan-DV, desenvolvida pelo Instituto Butantan, chegou aos braços dos brasileiros.
A parceria entre NIH/NIAID e Butantan foi oficializada em 2009, quando o instituto norte-americano cedeu as cepas atenuadas dos quatro sorotipos do vírus da dengue (DENV-1, DENV-2, DENV-3 e DENV-4) para que a vacina pudesse ser desenvolvida no Brasil. A tecnologia licenciada era fruto de uma década de pesquisa nos EUA e mais de 30 ensaios clínicos de fase 1, necessários para identificar a melhor forma de atenuar cada um dos quatro vírus. O objetivo era que todos eles provocassem uma resposta imune satisfatória, resultando em uma vacina capaz de proteger contra os quatro tipos da doença.
O cientista sênior do Laboratório de Doenças Virais do NIH/NIAID Stephen Whitehead, que liderou o desenvolvimento das cepas atenuadas, e a cientista e diretora do Centro de Pesquisa em Imunizações da Universidade Johns Hopkins, Anna Durbin, que conduziu os ensaios clínicos em parceria com o NIH/NIAID, contam ao Portal do Butantan os bastidores dessa jornada científica e como a colaboração com o Instituto Butantan ao longo de 20 anos foi fundamental para que a vacina chegasse àqueles que mais precisam.
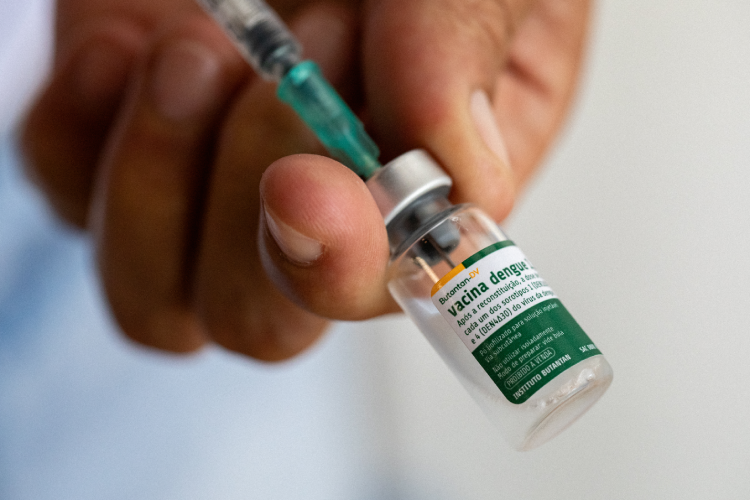
A vacina contra a dengue do Instituto Butantan é a primeira do mundo em dose única
Desenvolver um imunizante contra a dengue é um processo ainda mais complexo do que no caso de outras vacinas virais. Isso porque existem quatro tipos do vírus e a vacina deve, necessariamente, proteger contra todos eles. “Se a vacina não induz imunidade contra os quatro vírus, nós podemos acabar predispondo a pessoa a ter uma dengue mais grave no futuro, caso ela seja infectada”, explica Anna. Quando uma pessoa tem dengue, ela se torna imune àquele sorotipo que a infectou, mas não aos demais, e essa imunidade parcial aumenta o risco de desenvolver doença grave em uma segunda infecção.
Em uma vacina atenuada, os vírus precisam se replicar o suficiente para “estimular” uma infecção e fazer o organismo produzir anticorpos, mas sem causar a doença. Para chegar à formulação tetravalente, foi preciso estudar diversas formas de atenuar – ou “enfraquecer” – cada vírus. A técnica que funcionava muito bem para DENV-4, por exemplo, não era eficaz para DENV-2. “Nós customizamos as mutações genéticas para cada vírus, a fim de obter os candidatos monovalentes mais satisfatórios. Queríamos ter certeza de que tínhamos as cepas mais adequadas, que fossem seguras e imunogênicas”, conta Stephen Whitehead.
Cada cepa foi testada separadamente em modelos animais e, depois, em seres humanos. Foram 30 ensaios clínicos até que fosse possível determinar os quatro melhores candidatos para compor o imunizante. Para Anna Durbin, isso distingue a Butantan-DV das demais vacinas contra a dengue atualmente disponíveis: ela passou pela avaliação de múltiplos candidatos individuais e depois múltiplas formulações tetravalentes para chegar à mais promissora.

Stephen Whitehead é cientista sênior do Laboratório de Doenças Virais do NIH/NIAID
Outro desafio foi investigar qual seria a dosagem adequada de cada cepa para conferir proteção. Foram feitos quatro testes clínicos só com o componente DENV-4, por exemplo, para descobrir a melhor dose. “No caso do sorotipo 4, começamos com uma quantidade de 100.000 partículas de vírus, e acabamos descobrindo que apenas 1.000 partículas eram suficientes para induzir resposta. Isso foi muito importante em termos de custo-efetividade”, explica a pesquisadora da Universidade Johns Hopkins.
Na etapa final, os cientistas norte-americanos chegaram a duas formulações tetravalentes (as chamadas TV003 e TV005). Para determinar qual seria a mais segura e imunogênica para cruzar a linha de chegada, foi conduzido um novo ensaio clínico. Com uma única dose, a TV003 gerou anticorpos contra os quatro tipos da dengue em 90% dos voluntários e apresentou um melhor perfil de segurança. Foi com base nessa formulação que o Instituto Butantan desenvolveu a sua própria versão da vacina, análoga à TV003, entre 2009 e 2012, sob liderança de Neuza Frazatti Gallina, gerente de Desenvolvimento de Processos do Laboratório Piloto de Vacinas Virais.
“O Butantan teve confiança no produto antes mesmo de termos uma formulação final. É uma instituição que tem um histórico muito consolidado em desenvolvimento de vacinas, e sempre soubemos que seria uma parceria que daria certo”, resume Stephen.
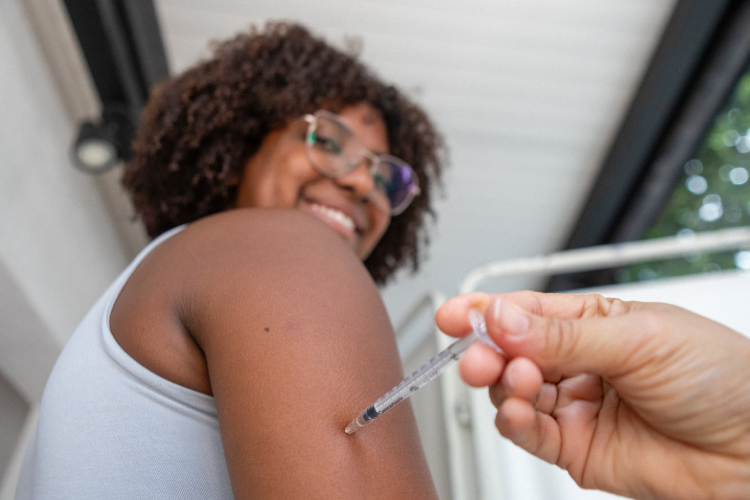
Os ensaios clínicos de fase 3 da vacina contaram com 16 mil voluntários de diferentes partes do Brasil
A preocupação com a segurança da vacina, especialmente em pessoas que nunca tiveram dengue, norteou os pesquisadores do NIH/NIAID e do Butantan do início ao fim do percurso – uma vez que outras vacinas disponibilizadas no mercado passaram a apresentar risco para essa população. Nos Estados Unidos, as equipes de Stephen e Anna desenvolveram um modelo de infecção humana controlada, também chamado de modelo de desafio, para confirmar que a imunidade conferida pela vacina era completa e não causaria maior risco de dengue grave após uma eventual infecção.
Já no Brasil, no ensaio clínico de fase 3 realizado com 16 mil voluntários, metade dos participantes incluídos tinha histórico de dengue, e a outra metade nunca havia tido contato com o vírus. Em cinco anos de acompanhamento, não foram observados sinais de preocupação em nenhum dos grupos, e a vacina demonstrou alta proteção contra dengue grave e com sinais de alarme, na faixa de 90%.
Outra vantagem clara, segundo a cientista Anna Durbin, é a aplicação do imunizante em apenas uma dose. “As vacinas não protegem as pessoas; o que protege é a vacinação. E com dose única, a vacina vai mais longe – você pode imunizar muito mais pessoas e não precisa se preocupar se elas voltam ao posto para receber a segunda dose. Elas já estarão protegidas”, afirma.

Anna Durbin é cientista e diretora do Centro de Pesquisa em Imunizações da Universidade Johns Hopkins
Os cientistas norte-americanos, que acompanharam o estudo da vacina da dengue desde a fase embrionária, acreditam que o imunizante, combinado a estratégias de controle do mosquito Aedes aegypti, poderá reduzir significativamente o número de casos e hospitalizações por dengue no Brasil nos próximos anos – e, futuramente, em outras regiões endêmicas.
Para isso, apontam que a vacina deve estar onde a doença acontece, e o acordo colaborativo entre NIH/NIAID e Butantan foi peça-chave nesse processo. “Esse trabalho foi da bancada ao produto e agora, com o Instituto Butantan, está indo além. Nos últimos 20 anos, diretoria após diretoria, nós estivemos aqui anualmente e o Butantan continuou levando esse projeto para frente e entendendo sua importância, porque é uma instituição comprometida com a saúde dos brasileiros”, destaca Stephen.
Anna reforça que metade da população mundial vive em áreas de risco para dengue, e que ainda há um longo caminho até que todas essas pessoas tenham acesso à vacinação. “Quando conseguirmos imunizar todo o público de risco, acredito que teremos um dos maiores impactos já vistos contra uma doença viral, semelhante ao que observamos com o sarampo, poliomielite e outras doenças imunopreveníveis. O peso no sistema de saúde vai diminuir drasticamente.”
Os pesquisadores ressaltam, ainda, a importância dos voluntários de cada ensaio clínico, que abriram caminho para que a vacina saísse do laboratório e chegasse à população com segurança e eficácia comprovadas. “São pessoas que doaram seu tempo, confiaram nos investigadores e acreditaram na ciência. Eles fizeram isso pelo bem da saúde pública e devemos nossos agradecimentos a eles”, diz Anna.
A Butantan-DV foi aprovada pela Agência Nacional de Vigilância Sanitária (Anvisa) em novembro de 2025 para o público de 12 a 59 anos, e começou a ser aplicada em janeiro deste ano. A vacinação foi iniciada nos municípios de Nova Lima (MG), Maranguape (CE) e Botucatu (SP), em um projeto piloto, e depois foi expandida para os profissionais de saúde da Atenção Primária. Demais públicos serão contemplados gradualmente.
Para Stephen e Anna, a expectativa é que, futuramente, o imunizante também possa ser disponibilizado para o público de 2 a 6 anos – já que a faixa etária demonstrou resultados promissores de segurança e eficácia durante a fase 3, inclusive em crianças sem exposição prévia ao vírus.
Atualmente, o Instituto Butantan conduz um ensaio clínico para avaliar a vacina na população de 60 a 79 anos. Os testes clínicos serão realizados ao longo de um ano em centros de pesquisa nos estados do Rio Grande do Sul e Paraná.

Anna Durbin e Stephen Whitehead durante homenagem recebida no Instituto Butantan
Na semana de celebração do aniversário de 125 anos do Instituto Butantan, Stephen Whitehead e Anna Durbin estiveram no Brasil e foram homenageados por suas contribuições no desenvolvimento da Butantan-DV, ao lado de profissionais do Instituto que também tiveram papel fundamental no estudo. A cerimônia aconteceu na terça (24/2), no Edifício Vital Brazil.
“A Butantan-DV é resultado do esforço não de uma só pessoa, de um só grupo, mas de um universo de pessoas que trabalharam diariamente por duas décadas para fazê-la acontecer. Tudo começou com uma descoberta feita pelo Stephen em seu laboratório, e juntos nós fomos capazes de levá-la adiante e transformá-la em um produto que salvará vidas”, resumiu o diretor do Instituto Butantan, Esper Kallás.



