



Um estudo da glândula salivar do carrapato-estrela (Amblyomma sculptum), famoso por transmitir a febre maculosa, mostrou outro lado desconhecido e inusitado do animal: moléculas com potencial para tratar doenças. A partir do DNA da glândula, cientistas do Butantan produziram uma proteína recombinante com atividade antitumoral, batizada de Amblyomin-X, que pode ajudar no desenvolvimento de tratamentos e de métodos de entrega de fármacos. O artigo sobre o assunto foi publicado na revista Frontiers in Molecular Biosciences e é uma revisão de 20 anos de pesquisas.
O trabalho foi coordenado pela pesquisadora Ana Marisa Chudzinski-Tavassi, diretora do Centro de Desenvolvimento e Inovação (CDI) do Butantan e coordenadora do Centro de Excelência para Descoberta de Novos Alvos Moleculares (CENTD). Até o momento, a proteína recombinante inteira mostrou capacidade de combater tumores em animais. A partir de porções da proteína, o grupo de cientistas produziu diferentes peptídeos sintéticos, que estão sendo testados separadamente em modelos de inflamação e dor.
Mais pesquisas ainda são necessárias para determinar a viabilidade industrial da proteína, mas a expectativa é que ela possa contribuir para o estudo de um futuro medicamento. Nesse momento, os cientistas buscam estabelecer formulações que mantenham as moléculas estáveis para diferentes aplicações.

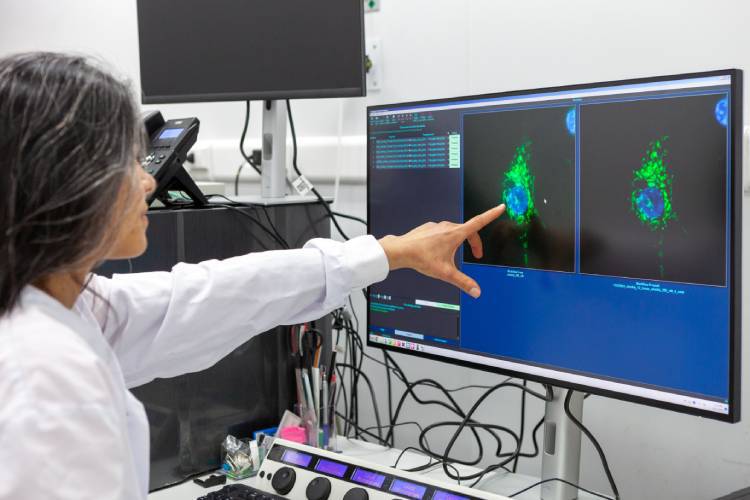
A pesquisadora Ana Marisa lidera o CENTD, onde a proteína foi desenvolvida
De acordo com Ana Marisa, não basta apenas identificar uma molécula com a atividade desejável, é preciso entender o mecanismo de ação, quais são seus alvos moleculares e desenvolver rotas tecnológicas escaláveis para sua obtenção – um esforço de muitos anos de estudo. “Nós utilizamos ferramentas de bioinformática e tecnologia de síntese de compostos para identificar quais são as partes essenciais da proteína e suas possíveis aplicações”, explica.
Nesse contexto, os pesquisadores determinaram no Amblyomin-X dois fragmentos de interesse: a porção responsável pela ação antitumoral (chamada domínio Kunitz) e a porção capaz de direcionar a proteína para dentro da célula tumoral (denominada C-terminal).
A porção C-terminal é uma molécula com função carreadora que tem sido testada em diferentes modelos celulares, para ajudar compostos terapêuticos de interesse a chegarem ao alvo desejado. Assim, o estudo do fragmento também pode ajudar no desenvolvimento de terapias mais específicas.
-a60c505315628ad7.jpg)
A biomédica Aline Ramos é pesquisadora do Butantan e primeira autora da revisão
Por que o carrapato-estrela?
O carrapato-estrela foi escolhido como objeto de estudo por ser um animal hematófago (que se alimenta de sangue). Para conseguir se nutrir, esses animais possuem um mecanismo que mantém o sangue do hospedeiro fluido: algumas moléculas em sua saliva têm ação anticoagulante, como é o caso de Amblyomin-X. Além de inibir a coagulação, a molécula também mostrou atividade antitumoral, levando os pesquisadores a testarem a proteína em tumores de animais.
É importante ressaltar que a molécula não oferece risco algum de causar febre maculosa, doença causada pela bactéria Rickettsia rickettsii. Apesar do Amblyomin-X ter sua origem no carrapato que transmite o patógeno, ele foi criado em laboratório a partir de uma sequência genética, ou seja, não vem diretamente do animal.
“A proteína Amblyomin-X não vem direto do carrapato em si: ela foi desenvolvida na forma recombinante em laboratório a partir da sequência de DNA extraída da glândula salivar do animal. A única forma de ter febre maculosa é entrando em contato direto com um carrapato infectado pelo microrganismo causador da doença”, esclarece a biomédica Aline Ramos Maia Lobba, colaboradora do artigo e pesquisadora do Butantan.
Como a proteína funciona
A molécula Amblyomin-X é descrita como um inibidor do tipo Kunitz, ou seja, possui um fragmento que inibe a ação de proteases (enzimas que degradam outras proteínas). Mais especificamente, o Amblyomin-X é capaz de inibir a atividade do proteassoma das células. Proteassoma é uma “maquinaria” responsável por degradar as proteínas que não são necessárias à vida da célula, fazendo uma espécie de limpeza e ajudando a regular os processos celulares.
“Quando essa ‘máquina’ para de funcionar, a célula acumula muitas proteínas indesejáveis, na forma de agregados, o que acaba levando à morte celular”, diz Aline.
Além de bloquear o proteassoma, a substância é capaz de ativar a resposta imunológica. Mais testes estão sendo feitos em células para descobrir como exatamente a proteína pode modular essa resposta.
Resultados iniciais
Em testes preliminares, o Amblyomin-X induziu a morte de diferentes linhagens de células cancerosas, especialmente as derivadas de tumores sólidos. A proteína também foi eficaz contra metástase: reduziu em 60% os nódulos metastáticos nos pulmões, rins e linfonodos em animais de pequeno porte. Já no melanoma equino espontâneo (em cavalos), o tratamento reduziu o volume do tumor em 75%. Além disso, diferente de outras substâncias semelhantes já estudadas, Amblyomin-X não causou hemorragia nos animais, mesmo em repetidas doses.
Testes de segurança em animais (provas de conceito e pré-clínicos) também indicaram que a proteína recombinante é muito bem tolerada e não apresenta toxicidade, mesmo em doses mais elevadas (30 vezes a dose efetiva). “Em animais saudáveis, a molécula é eliminada rapidamente pela urina. Já quando administrada em animais com câncer, ela age direto na região do tumor, sem afetar os tecidos saudáveis”, explica Aline.
Futuramente, o conhecimento sobre a seletividade da proteína pode ajudar no desenvolvimento de fármacos menos tóxicos e mais eficientes. Segundo Aline, é difícil obter moléculas que sejam específicas apenas para as células cancerosas. “A maioria dos atuais tratamentos freia a divisão celular, atingindo não só as células tumorais, mas também as saudáveis. Por isso há efeitos colaterais como queda de cabelo e perda de massa muscular, por exemplo.”
Para conseguir transformar o Amblyomin-X em um produto viável, os próximos passos incluem investir na formulação para garantir a estabilidade da molécula inteira e dar continuidade aos testes dos fragmentos (peptídeos) para otimizá-los, de acordo com Ana Marisa.
Reportagem: Aline Tavares
Fotos: José Felipe Batista/Comunicação Butantan



