



Reportagem: Natasha Pinelli
Imagens: Comunicação Butantan e José Felipe Batista/Comunicação Butantan
A recente aprovação pela Agência Nacional de Vigilância Sanitária (Anvisa) da Butantan-DV, vacina desenvolvida pelo Instituto Butantan que contém os quatro sorotipos da dengue, é um marco da ciência brasileira. Em 2024, a doença atingiu recordes históricos, superando mais de 6,5 milhões de casos prováveis e 6.321 óbitos no país, e se consolidou como um dos principais desafios mundiais de saúde pública.
A obtenção do registro representa, também, a coroação de 15 anos intensos de trabalho científico e industrial que resultaram no primeiro imunizante inteiramente concebido pelo Butantan. Dos primeiros passos do produto na bancada, até a criação de uma fábrica dedicada que nunca para, foram necessárias 17 receitas de formulação, 12 condições de liofilização em escala industrial, além de inúmeros experimentos e testes de qualidade.
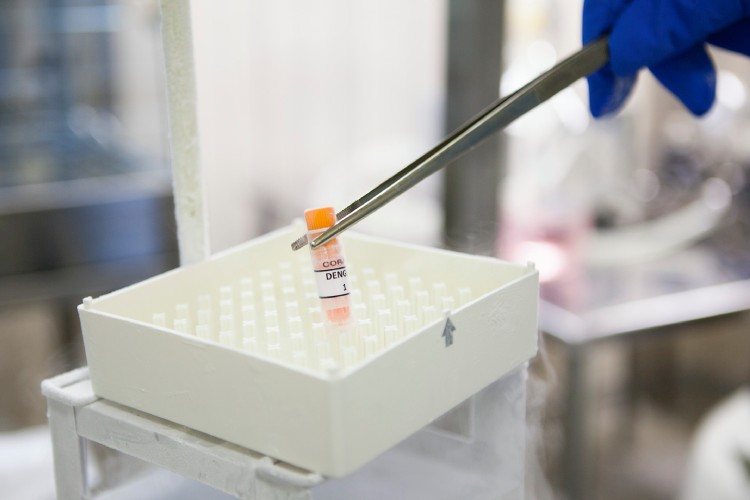
Tetravalente: a Butantan-DV reúne os quatro sorotipos da dengue (Foto: Comunicação Butantan)
“A fabricação da Butantan-DV envolve uma cadeia extensa e altamente complexa, em que cada etapa precisa funcionar em perfeita sincronia para garantir o resultado final. É um sistema de engrenagens que deve operar com precisão para alcançar o que chamamos de ‘vacina ideal’: aquela que contém exatamente o necessário para reproduzir, com segurança e eficácia, os parâmetros estabelecidos nos estudos clínicos”, aponta o diretor técnico de Produção da Vacina da Dengue, Antonio Cesar Pereira da Silva.
Com o aval da Anvisa, um milhão de doses do imunizante já prontas estão cada vez mais próximas de chegarem aos braços dos brasileiros. A seguir, conheça os bastidores dessa jornada de pesquisa e desenvolvimento e entenda o que torna o imunizante do Instituto Butantan tão especial e desafiador.

A transição do processo de liofilização em laboratório para escala industrial foi um dos mais desafiadores (Foto: Comunicação Butantan)
Foi no ano de 2010 que o projeto da vacina da dengue começou a ser semeado no Instituto Butantan. Na época, o país passava por uma grave epidemia da doença, com mais de 1 milhão de casos registrados – quase o triplo de notificações quando comparado a 2009.
A árdua tarefa foi designada à gerente de Desenvolvimento de Processos do Laboratório Piloto de Vacinas Virais, Neuza Frazatti Gallina. Com o auxílio de sua equipe, a especialista passou a trabalhar na formulação do imunizante, utilizando cepas atenuadas dos quatro sorotipos do vírus da dengue circulantes no mundo (DENV-1, DENV-2, DENV-3 e DENV-4) que haviam sido doadas pelo Instituto Nacional de Saúde dos Estados Unidos (NIH).
O uso dessas cepas atenuadas – ou seja, nas quais foi “deletada” parte dos genes responsáveis pela replicação do vírus – permite que a vacina simule no organismo uma infecção “natural”, mas sem desencadear a doença de fato. A robustez dessa resposta imunológica é o que torna viável o esquema de vacinação em dose única: um diferencial estratégico que simplifica a logística das campanhas e contribui para uma maior adesão popular.
“A imunização é um pacto social: só estamos protegidos quando atingimos um percentual mínimo de pessoas vacinadas. Quando você tem um produto de dose única, essa cobertura é alcançada mais rapidamente, com uma única ida ao posto de saúde. Isso é especialmente vantajoso em um cenário de hesitação vacinal”, afirma a diretora de Assuntos Regulatórios, Qualidade e Escritório de Projetos do Butantan, Rosilane de Aquino Silva.
Os benefícios da dose única foram descritos em um relatório publicado por pesquisadores do Reino Unido na Human Vaccines & Immunotherapeutics, em 2018. O estudo apontou que programas de imunização com menos doses estão associados a uma melhor cobertura vacinal e menos impactos na economia.
Outra característica fundamental da Butantan-DV é ser desenvolvida com os quatro sorotipos do vírus da dengue, o que a torna uma vacina tetravalente. Essa abrangência é essencial, pois uma pessoa infectada por um sorotipo e, posteriormente, exposta a outro pode desenvolver uma resposta imunológica desequilibrada, aumentando o risco de formas graves da doença.
É justamente na necessidade de equilibrar a combinação dessas diferentes cepas que reside parte da complexidade do imunizante. Em termos simples, os pesquisadores precisaram descobrir quatro números mágicos: a quantidade de partículas virais de cada sorotipo em uma dose da vacina, a fim de que o produto fosse capaz de desencadear uma resposta imunológica eficaz e equilibrada no organismo.
“São esses números que vão nortear todas as etapas de produção: desde o volume obtido de cada uma das cepas no processo produtivo do Insumo Farmacêutico Ativo [IFA], até a quantidade utilizada na formulação e liofilização do produto”, explica o gerente de Produção da Vacina da Dengue, Alexandre Gonçalves de Rezende.
Os imunizantes liofilizados têm aparência semelhante a uma pastilha – por isso, no momento da administração, a Butantan-DV precisará ser reconstituída com o auxílio de um diluente. O processo de secagem a frio que dá origem à vacina da dengue é essencial para preservar a integridade do produto, garantindo que a concentração de partículas virais permaneça estável ao longo do tempo.
A versão liofilizada do imunizante tem validade estendida e pode ser armazenada em refrigeradores convencionais, entre 2 °C e 8 °C, o que facilita o transporte e a distribuição. Alexandre Gonçalves de Rezende explica que a formulação líquida exigiria uma cadeia de frio muito mais complexa, pois qualquer variação de temperatura poderia comprometer a estabilidade do vírus atenuado e reduzir a resposta imunológica ao produto.

A vacina da dengue do Instituto Butantan é feita com vírus vivo atenuado (Foto: Comunicação Butantan)
Enquanto o Instituto Butantan trabalhava na formulação do seu imunizante contra a dengue, o NIH já dava início à fase 1 dos estudos clínicos da sua própria candidata vacinal, nos Estados Unidos. Nessa etapa, o objetivo era avaliar a segurança e a tolerabilidade do produto em seres humanos. O estudo foi finalizado em 2012, com resultados positivos: a vacina americana foi considerada segura e não foram observados efeitos adversos graves.
Por mais que os protótipos do NIH e do Butantan não fossem exatamente os mesmos, a similaridade entre eles – como o uso das mesmas cepas atenuadas – permitiu que o Instituto utilizasse os dados obtidos pela agência na fase 1 de ensaios clínicos e avançasse diretamente para um estudo de fase 2, iniciado em 2013. O foco da nova etapa foi avaliar a eficácia preliminar da vacina, assim como continuar o monitoramento de segurança e tolerabilidade, dessa vez em uma população altamente exposta à doença.
Após a conclusão dessa etapa, o Instituto Butantan colocou de pé um dos maiores ensaios clínicos já realizados no país: o estudo de fase 3 da sua candidata à vacina da dengue. Lançada em 2016, a pesquisa foi conduzida em parceria com 16 centros espalhados por todo o país e envolveu cerca de 17 mil voluntários, que foram acompanhados ao longo de cinco anos.
O ensaio foi essencial para comprovar a eficácia e a segurança do imunizante, consolidando os resultados obtidos nas fases anteriores, além de fornecer a base necessária para que o Instituto iniciasse os trâmites de registro do produto junto à Anvisa.

Inaugurada em 2018, a planta da Produção de Vacina Dengue possui 2.550m² (Foto: Comunicação Butantan)
Com o sucesso dos ensaios clínicos, o desafio seguinte foi transpor o processo produtivo da vacina, até então feito em um laboratório piloto, para uma fábrica de alta escalabilidade. Inaugurado em 2018 e com cerca de 2.550 metros quadrados de área produtiva, o prédio de Produção da Vacina Dengue se tornou o coração produtivo da Butantan-DV.
Porém, a etapa de escalonamento estava longe de ser uma simples replicação do processo estabelecido em laboratório, apenas utilizando maquinários maiores. “Na prática, passamos a lidar com um volume muito maior de produto, um outro liofilizador, uma outra linha de envase, o que se refletiu na necessidade de alguns ajustes produtivos”, pontua a gerente de Produção da Butantan-DV, Daniella Ventini.
De acordo com os especialistas do Instituto, um dos pontos mais complexos dessa transição foi, justamente, a etapa de liofilização, uma vez que a “receita” utilizada no maquinário piloto não pôde ser aplicada nos equipamentos de grande porte da planta industrial. Foram avaliadas 12 condições distintas até atingir o ciclo ideal. “Cada pequeno ajuste precisou ser validado e revalidado para garantir que a qualidade da vacina que foi testada nos ensaios clínicos permanecesse inalterada”, reforça Antonio Cesar Pereira.
Paralelamente a esse período de estruturação do prédio de Produção da Vacina Dengue, o Instituto firmou um acordo de parceria estratégica com a farmacêutica MSD, com o objetivo de compartilhar dados clínicos e tecnológicos – por também utilizar as mesmas cepas atenuadas fornecidas pelo NIH, a empresa americana possui um produto análogo à Butantan-DV.
“O acordo permitiu que a MSD utilizasse as evidências geradas pelo Butantan no ensaio clínico conduzido no Brasil, enquanto nós pudemos incorporar melhorias de processo e parâmetros produtivos na nossa linha de fabricação”, esclarece Daniella Ventini. Essa colaboração internacional fortaleceu a vacina e acelerou os ajustes necessários para ampliar a produção em escala industrial.

Parte da equipe de produção, responsável pela fabricação da vacina da dengue (Foto: José Felipe Batista/Comunicação Butantan)
As adaptações realizadas na fábrica do Butantan demandaram a estruturação de um estudo de consistência clínica da vacina. Os testes foram conduzidos em cerca de 700 voluntários e o objetivo foi comprovar que o imunizante contra a dengue produzido na planta industrial apresentava resultados equivalentes ao produto desenvolvido previamente em escala piloto.
Com o sucesso de mais essa etapa, o Butantan pôde avançar para a validação interna do processo produtivo – mais um ponto essencial para o registro sanitário. Nessa fase, foi preciso comprovar que toda a jornada de fabricação do imunizante é reprodutível, segura e consistente. “Isso é feito por meio da avaliação de três lotes do produto desenvolvidos consecutivamente em condições controladas, simulando cenários críticos e garantindo que todas as doses formuladas atendam aos mesmos padrões de qualidade”, explica o diretor técnico de Produção da Vacina da Dengue.
No caso da Butantan-DV, a validação do Insumo Farmacêutico Ativo (IFA) foi concluída em 2021, e a do produto acabado – que contempla as fases de formulação, envase e liofilização – foi finalizada em 2024. Os marcos permitiram à instituição compilar o dossiê de registro da vacina da dengue, submetido à Anvisa no final de 2024 e, agora, finalmente aprovado.



